Les principes généraux du traitement
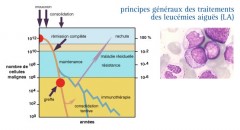
LE TRAITEMENT D’INDUCTION POUR OBTENIR UNE RÉMISSION
SON OBJECTIF
Le but de la chimiothérapie très intensive d’induction est d'obtenir la rémission complète de la maladie.
LES PRINCIPES DE BASE
Ils faut abaisser le plus rapidement possible la masse des cellules leucémiques au prix d’une aplasie médullaire de 2 à 4 semaines après la fin du cycle d’induction de 5 à 10 jours.
Les cellules tumorales résiduelles seront éliminées au cours des cycles de chimiothérapie de consolidation.
Le traitement d'induction, en supprimant plus de 99 % des cellules malignes, va permettre de rétablir un fonctionnement normal de la moelle osseuse et améliorer l'état général.
Si ce traitement réussit, vous serez alors en rémission complète. L’obtention d’une rémission complète est de bon augure pour la suite du traitement...
LA PROPHYLAXIE NEURO-MÉNINGÉE
Les faits...
De 30 à 40 % des rechutes initiales des leucémies aiguës lymphoblastiques (LAL) sont des rechutes méningées. Le risque est plus élevé en cas de leucémies à cellules « T », de forte hyperleucocytose et de certaines anomalies génétiques. De ce fait, la prophylaxie méningée a pour objectif de détruire d’éventuelles localisations de la maladie dans le système nerveux central (SNC).
Pourquoi?
La plupart des médicaments de chimiothérapie ne franchissent pas ou mal la barrière hémato-encéphalique. Cela veut dire que ces médicaments ne peuvent pas diffuser dans le liquide céphalo spinal (LCS) et donc détruire les cellules malignes présentes autour et dans le cerveau ou la moelle épinière. Les spécialistes parlent alors de zones « sanctuaires ».
Afin d'éviter une rechute de la leucémie à partir de cellules malignes des enveloppes du cerveau (les méninges), une chimiothérapie locale appelée « prophylaxie neuro-méningée » sera systématiquement faite.
Comment ?
Ce traitement est particulièrement important dans le cas des leucémies lymphoblastiques et plusieurs options sont possibles :
- Une radiothérapie appliquée sur le crâne dosée entre 12 et 18 Gy, plus rarement de nos jours.
- Une chimiothérapie comprenant du méthotrexate par voie injectable associée à du méthotrexate administré par ponction lombaire (voie intrathécale) en prenant beaucoup de précautions pour éviter d’ensemencer avec des cellules leucémiques le LCS
EN PRATIQUE….
Cette première phase du traitement nécessite une hospitalisation en chambre stérile pendant environ un mois car il implique une phase d'aplasie liée à la chimiothérapie de 3 à 4 semaines.
Il comporte une ou deux cures de polychimiothérapie. La nature de la chimiothérapie dépend du type de leucémie et de votre âge mais comprend toujours une anthracycline.
L'induction thérapeutique comprend quatre étapes :
- La phase de réduction du nombre cellules tumorales « blastique »
- La phase d'aplasie liée au traitement
- La phase de régénération, qui est courte
- La rémission.
Trois critères d'une rémission complète...
- Disparition des blastes : < 5 % dans la moelle et le sang
- Numération formule sanguine (NFS) normale
- Disparition des symptômes
PHASE 2 : TRAITEMENT DE CONSOLIDATION (INTENSIFICATION)
LE CONCEPT DE MALADIE RÉSIDUELLE
Quelques chiffres...
Dans la plupart des cas, le nombre de cellules leucémiques lors du diagnostic est compris entre 1011 et 1012 cellules (100 g à 1 kg de tissu). Dès que le nombre de cellules est en dessous de 1010 , soit environ 10 g de tissu, les cellules leucémiques ne sont plus détectées par l’examen du sang, NFS et de la moelle. Dans ce cas, le patient est alors considéré en rémission hématologique complète.
Supposons que 99 % d'un milliard de cellules malignes ont été détruites, il en reste encore un million dans le corps...
Bien que plus de 90 % des cellules soient très sensibles à la chimiothérapie, les cellules leucémiques survivantes ne peuvent pas, encore, être détectées dans la moelle osseuse car sont présentes à des taux inférieurs, aux limites de la détection des techniques cytologiques. Ceci explique les rechutes, si rien n’est fait pour les prévenir. Pour cette raison, les protocoles de chimiothérapie proposent des traitements de « consolidation » de cette rémission pour prévenir une rechute précoce, surtout en cas de leucémies myéloblastiques.
Les nouvelles techniques d'évaluation de la maladie résiduelle
Actuellement, deux techniques sont validées pour rechercher les cellules leucémiques résiduelles. La sensibilité des techniques en cytométrie de flux et de PCR permettent de détecter une cellule parmi un million de cellules.
LES TROIS OPTIONS
Une allogreffe moelle osseuse
Elle est proposée chez les patients âgés de moins de 55 ans, s’il existe un donneur HLA identique. Elle implique un conditionnement standard ou atténué.
Une autogreffe de moelle osseuse
Dans ce cas, les cellules souches du patient qui seront réinjectées, sont prélevées à la fin de l'aplasie associée au traitement de consolidation. par la suite, on effectue une consolidation par chimiothérapie et souvent irradiation du corps entier, ou conditionnement, suivie de réinjection des cellules-souches, pour éviter une aplasie définitive.
Une chimiothérapie de consolidation
Deux à trois cures intensives de chimiothérapie, aplasiantes, qui reprennent le protocole initial et nécessitent, tous les 3 ou 4 mois, une hospitalisation en milieu spécialisé sur 4 à 6 mois sont nécessaires.
Les produits utilisés sont les mêmes que ceux de la cure d'induction.
Cette phase du traitement dure 6 mois pour les leucémies lymphoblastiques. Le traitement s’effectue en hôpital de jour ou en service spécialisé, en cas de greffe de moelle.
Les effets secondaires de cette cure de consolidation sont identiques à celle du premier traitement : aplasie prolongée, avec ses risques infectieux et hémorragiques.
Les facteurs suivants sont reconnus pour influer sur le pronostic de la maladie
- L'âge
- L'importance du syndrome tumoral
- L'existence ou non de localisations neuro-méningées
- Le nombre de globules blancs (leucocytose), en particulier s'il est supérieur à 40 000/mm 3
- Un sous-type cytologique défavorable: LAL de meilleur pronostic qu'une LAM ; LAM1 ou une LAM2 de meilleur pronostic qu'une LAM4 ou une LAM5 ; LA inclassables, bi- ou multi-phénotypiques
- Un caryotype de bon pronostic : translocation t(15-17), inversion 16, translocation t (8,21) de la LAM2 ou un de moins bon pronostic : anomalies du chromosome 5 et 7 ; existence de cassures chromosomiques multiples
- La réponse initiale à la chimiothérapie / Une rémission complète lors de la première cure de chimiothérapie est un élément favorable
PHASE 3 : LE TRAITEMENT D'ENTRETIEN
Il n'est pas nécessaire, en cas de greffe de moelle.
Dans les autres cas, le traitement d'entretien se fait en ambulatoire et fait appel à une association de méthotrexate et de 6-mercaptopurine (Purinethol™).
L’objectif du traitement est d’obtenir un nombre de globules blancs inférieur à 3 x 10 9 /L et de polynucléaires neutrophiles situé entre 0,5 et 1,5x10 9 /L.
Un schéma « mixte » Il s’agit, dans ce cas, d’un traitement par chimiothérapie continue à base de méthotrexate et de 6 mercaptopurine, associé à des ré-inductions à l’occasion d'hospitalisations, courtes mais régulières
Cette phase du traitement dure de 1,5 à 2 ans.
Important durant le traitement d'entretien...
Une contraception efficace durant la chimiothérapie et jusqu’à 1 an après la fin de celle-ci pour les femmes en âge de procréer
Les rapports sexuels doivent être protégés afin d’éviter le passage de chimiothérapie toxique et de prévenir les infections sexuellement transmissibles
Le traitement des rechutes
LA GUÉRISON
Elle est affirmée, 5 ans après obtention de la réponse complète. Les résultats des traitements, à l’heure actuelle sont de :
- 50 à 60 % des enfants avec la chimiothérapie seule
- 30 % des adultes avec la chimiothérapie seule
- 50 % des adultes avec allogreffe de cellules souches hématopoïétiques.
LES RECHUTES
En dépit des traitements de consolidation et d'intensification, chez les patients qui ne reçoivent pas d'allogreffe, le risque de rechute reste de 30 à 80 %. Ces rechutes surviennent généralement dans les deux premières années qui suivent la mise en rémission. Les rechutes sont plus souvent réfractaires au traitement, et le sont d'autant plus qu'elles surviennent précocement.
Il n'y a pas de traitement standard des rechutes. Si elles surviennent tardivement, un traitement, analogue à celui donné lors de l'induction, peut être proposé. Des protocoles de traitements comportant de nouveaux médicaments peuvent être proposés dans le cadre d'essais thérapeutiques.
VOUS ÊTES ENCEINTE...
Les leucémies aiguës compliquent une grossesse sur 100 000 grossesses.
Le traitement repose sur la chimiothérapie, de ce fait, la découverte d'une leucémie aiguë au premier trimestre nécessite une polychimiothérapie d'urgence et impose une interruption de grossesse.
L'histoire naturelle et le pronostic de leucémie ne sont pas modifiés par la grossesse. Le pronostic maternel est moins favorable, mais à tendance à s'améliorer.
Mise à jour
5 octobre 2016

