Une leucémie
La publication de P.H. Nowell & D.A. Hungerford (Science 1960)
LE PREMIER MARQUEUR CHROMOSOMIQUE...
Une anomalie chromosomique acquise, le chromosome dit de Philadelphie (Ph1), est caractéristique de la LMC. Le terme Philadelphie vient du fait que le raccourcissement du bras long du chromosome 22 a été décrit à Philadelphie, en 1960, par PH Nowell et DA Hungerford (Science 1960;132:1497 ).
Cette translocation réciproque entre les bras longs des chromosomes 9 et 22 a constitué le premier marqueur chromosomique décrit dans une affection maligne.
LE CHROMOSOME PHILADELPHIE
Le chromosome Philadelphie est retrouvé chez 95 % des patients atteints d’une LMC et dans certaines leucémies aiguës myéloblastiques (LAM).
Cette anomalie chromosomique, acquise, est due à une translocation lors de la division cellulaire. Une translocation est un échange de matériel chromosomique entre des chromosomes non homologues, c'est-à-dire n'appartenant pas à la même paire.
Le chromosome Philadelphie
Définition
- Sur le chromosome 9 en amont de l’exon 2 de l’oncogène d'Abelson c-ABL localisé en position 9q34. Son nom est dérivé de son homologue viral, le gène Abelson ( v-ABL ), responsable d’une forme de leucémie chez la souris.
- Sur le chromosome 22, au niveau du gène BCR ( Break Cluster Region ). Le gène BCR , positionné sur le bras long du chromosome 22, a été découvert en clonant la région appelée Major-Breakpoint Cluster Region d'où M-BCR où ont lieu la majorité des points de cassure.
La proximité des deux gènes dans les cellules CD34+ est probablement un facteur favorisant. Cependant, ce réarrangement moléculaire acquis et spécifique ne paraît pas seul en cause dans la genèse de la maladie, la détection de transcrits de BCR-ABL chez des sujets sains, n'étant pas exceptionnelle.
UN GÈNE DE FUSION HYBRIDE BCR/ABL
Les conséquences
L'expression de l'oncoprotéine p210(bcr/abl)
- Une activation constitutive de signaux de transduction cellulaire mitogènes affectant la voie RAS-MAP kinase, la voie JACK-STAT, la voie Myc, et la voie FAK, aboutissant à une stimulation de la prolifération cellulaire
- Une réduction voire le blocage des fonctions d'apoptose via la voie du Bcl2 et celle de la phosphorylation de Bad
Une expansion du compartiment myéloïde...
La moelle osseuse fabrique alors des globules blancs à un rythme effréné et les déverse dans le sang et leur nombre va rapidement passer de 4 000 à 150 000 par mm 3 !
Par la suite...
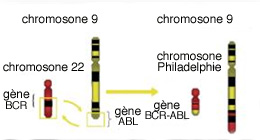
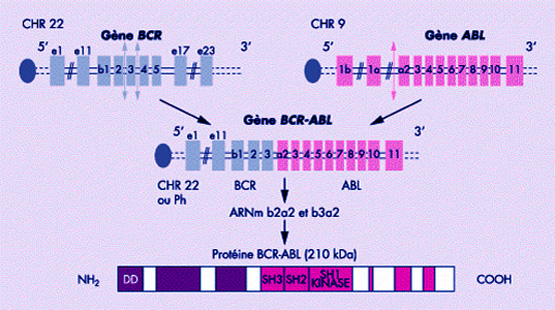
Conséquence de la translocation
t(9;22)(q34;q11)
⇓
Gène hybride bcr-abl
⇓
Protéine anormale bcr-abl (210 Kd)
à forte activité tyrosine kinase non régulée
⇓
Stimulation de la prolifération cellulaire
Mise à jour
25 mai 2023

