Le bilan initial
LA CONSULTATION INITIALE CHEZ LE SPECIALISTE
S'il y a des raisons de suspecter un cancer, vous serez examiné par un ou plusieurs spécialistes : un gastro-entérologue, un hépatologue (spécialiste du foie), un oncologue et/ou par un chirurgien.
Dans tous les cas, la première étape de l'évaluation consiste en un recensement complet de vos antécédents médicaux et l'examen clinique. Au cours de l'entretien Le médecin vous demandera de préciser les symptômes que vous ressentez. Il vous interrogera sur votre passé médical et sur tous vos autres problèmes de santé.
Plus particulièrement, il recherchera si vous avez contracté une hépatite, si vous avez été transfusé ou quelles sont vos habitudes en matière de consommation d’alcool.
Le foie est accessible à l'examen clinique dans la partie haute et droite de l'abdomen. Les médecins rechercheront l’existence d’un gros foie et ils apprécieront sa taille et sa consistance. Parfois ils pourront sentir la présence d’un ou plusieurs nodules.
Le cancer du foie pouvant s'étendre aux organes avoisinants, les autres organes de l'abdomen et les aires ganglionnaires seront aussi minutieusement examinés.
Les examens de sang
POURQUOI ?
Le bilan hépatique est un bilan sanguin couramment prescrit, utilisé pour évaluer les différentes fonctions du foie ou mettre en évidence une atteinte hépatique. L’objectif du bilan sanguin est d’étudier les trois fonctions majeures du foie et de rechercher si vous avez fait une hépatite B ou C
LE BILAN HEPATIQUE
Les tests
Tout d'abord, pour être interprétable, il doit être complet et comporter l'évaluation des principales fonctions hépatiques :
- L’alanine aminotransférase (ALAT, SGPT) est une enzyme qui se trouve majoritairement dans le foie. Une élévation de son taux sérique signifie souvent une atteinte hépatocellulaire. Ce test est beaucoup plus spécifique d’une lésion hépatique que l’ASAT. L’importance de l’augmentation est dite légère lorsque le taux est < 5 fois la normale ; intermédiaire 5 à 15 fois la normale et élevée > 15 fois la normale.
- L’aspartate aminotransférase (ASAT, SGOT) est plus ubiquitaire et peu spécifique et se trouve non seulement dans le foie mais également dans d’autres organes
- La phosphatase alcaline (PA) se trouve majoritairement dans le foie et les os. Tout comme la gamma GT (GGT), elle est un marqueur de cholestase. Le dosage concomitant de la GGT permet de déterminer l’origine de l’élévation de la PA : si celle-ci est normale, l’origine est osseuse, sinon elle est hépatique
- La recherche de stigmates d'une hépatite B ou C
Les résultats
L'insuffisance des fonctions métaboliques du foie (insuffisance hépatocellulaire) entraîne la diminution de très nombreuses protéines du sang. Le dosage de l'albumine est avec le taux de prothrombine, le témoin le plus utilisé.
En cas de destruction des cellules hépatiques (cytolyse ou nécrose), le taux dans le sang des transaminases ALAT ou SGPT et ASAT ou SGOT est élevé.
En cas de cholestase, la bilirubine, les phosphatases alcalines, ainsi que la gamma-glutamyl-transpeptidase (Gamma-GT) sont élevés.
LE DOSAGE DES MARQUEURS TUMORAUX
Le dosage de l'alpha-foeto-protéine (AFP) est très important, mais il n’est pas spécifique de la maladie.
Une élévation de l'alpha-foeto-protéine dans le sang, surtout si la valeur est supérieure à 500 ng/ml, est très évocatrice d'un cancer du foie chez un patient souffrant d'une cirrhose. Cependant, une telle élévation ne survient que dans environ 50 % des cas. Dans environ 30 % des cas, des chiffres situés entre 20 et 500 ng/ml sont observés. Dans 20 % des cas, la valeur est normale.
Au cours de la surveillance d'une cirrhose, la mise en évidence d'une élévation modérée de l'alpha-foeto-protéine doit faire pratiquer des dosages répétés pour confirmer ou infirmer le diagnostic. Une échographie abdominale sera réalisée en parallèle de ces dosages répétés.
@ Pour plus de détails: Marqueurs tumoraux
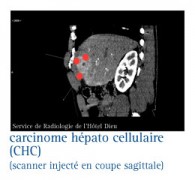
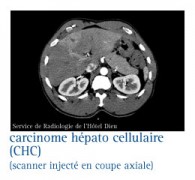
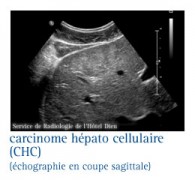
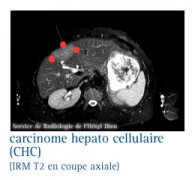
L'imagerie pour répondre à la question : le nodule est-il cancéreux
IMPORTANT ...
La caractérisation du ou des nodule(s) repose sur l’examen de leur vascularisation. La standardisation de l’imagerie (technique et interprétation) est un enjeu important qui a conduit à la création du système LI-RADS (Liver Imaging Reporting and Data System) qui est une façon de standardiser le compte rendu radiologique en imagerie hépatique chez des patients à risque de cancer du foie.
L'ÉCHOGRAPHIE
C'est un examen indolore utilisant les propriétés des ultrasons à se réfléchir sur les différentes structures anatomiques. Cette technique permet de repérer une masse hypoéchogène (diminution de l'écho), remaniée. Son interprétation est parfois difficile car la structure du foie est déjà remaniée par la cirrhose. L'examen recherche la présence d'un ou plusieurs nodules au sein du foie.
Le signe échographique très suspect de carcinome hépatocellulaire surajouté à la cirrhose est l'existence d'une thrombose associée de la veine porte qui est détectée à l'aide d'un examen associé Doppler.
L'échographie de contraste est une technique récente permettant de caractériser la vascularisation d’un nodule. Sa sensibilité pour dépister l’hypervascularisation à la phase artérielle est supérieure à celle du scanner.
LE SCANNER
Le scanner hélicoïdal (TDM) abdominal avec triple acquisition artérielle, portale et tardive
C’est le procédé plus récent et plus précis car il montre le foie, les ganglions lymphatiques et d'autres parties du corps avec une grande précision, le scanner peut aussi préciser si le cancer s'est étendu du foie vers les autres organes de l'abdomen.
Au cours de cet examen, les rayons X tournent constamment autour du patient et de part ce procédé, la méthode est plus efficace et le temps d'examen de l'abdomen est réduit de deux minutes à 20 ou 30 secondes par le scanner hélicoïdal.
Des images en trois dimensions sont produites à la place des images en deux dimensions du scanner conventionnel.
Le signe le plus évocateur de cancer est l’existence d’un nodule hypervascularisé au temps artériel précoce (wash-in) avec lavage (wash-out : hypodensité ou hypo-intensité par rapport au parenchyme hépatique non tumoral) à la phase portale ou à la phase tardive par rapport au parenchyme non-tumoral. Ceci traduit la disparition de la vascularisation par la veine porte au profit d'une vascularisation par l'artère hépatique exclusive.
Le scanner à deux phases
Cette technique nécessite la présence de deux scanners synchronisés. L'intérêt de cette technique est de pouvoir être utilisée au moment où l'efficacité du produit de contraste est optimale.
L'IRM
L’imagerie à résonance magnétique est un examen qui permet de faire la même chose qu'une coupe d’organe. Contrairement aux rayons X aucune radiation n'est utilisée dans cette technique.
L'appareil fonctionne au moyen d'un aimant et d'ondes radio. L'IRM avec injection de ferrites montre des nodules vides de fer.
Cette technique peut être utile sur un foie remanié par une cirrhose associée. Ses performances sont un peu supérieures au scanner, en termes de sensibilité, pour la détection et la caractérisation des nodules, permettant notamment de distinguer nodule de régénération et nodule cancéreux.
L'IRM est utile lorsque le scanner n’est pas concluant. Néanmoins, il donne au chirurgien des renseignements morphologiques moins précis que le scanner.
LA TEP-scan 18F-FDG:CHOLINE
Ces examens sont peu utiles actuellement. Néanmoins, l'utilisation d'un autre traceur, la 11C-choline, pourrait être utile pour détecter des tumeurs bien différenciées.
La ponction biopsie hépatique
POURQUOI ?
La biopsie est utile au diagnostic
Un certain nombre de nodules correspond, après examen histologique, à des nodules hépatocytaires bénins ou à des lésions non hépatocytaires (hémangiomes, cholangiocarcinomes). La cirrhose est un état pré-néoplasique où se développent des nodules cirrhotiques dont certains, les nodules dysplasiques, ont un potentiel certain de malignité, et dont la connaissance précise est importante pour la prise en charge.
La biopsie est importante pour la caractérisation des nodules et pour identifier ceux cancéreux. Elle est aussi importante pour préciser la stratégie thérapeutique. Ainsi, la caractérisation des tumeurs devient un élément indispensable pour le traitement et plus particulièrement si une greffe du foie est envisagée.
De fait, les tumeurs malignes du foie sont très hétérogènes et leur classification en sous-types histologiques et génétiques est devenue primordiale pour le traitement.
La biopsie est utile pour l’évaluation pronostique
Ceci repose sur le fait que le grade de différenciation tumorale est un facteur validé pronostique de la maladie.
COMMENT ?
Elle consiste à prélever un petit bout de tissu hépatique, à l'aide d'une aiguille (voie transpariètale) pour l'analyser ensuite au microscope.
La biopsie utilisant des aiguilles de 14 à 18 G est utilisée préférentiellement car elle fournit un matériel tissulaire permettant une analyse histologique.
Si une transplantation hépatique est envisagée une protection du trajet pariétal sera obtenue par l'utilisation d'une aiguille co-axiale, en raison du risque d’essaimage du trajet de ponction.
En cas de traitement percutané, une biopsie par la même aiguille introductrice doit être faite lors de la première séance.
Les contre-indications de la ponction biopsie hépatique par voie trans-pariétale sont surtout les troubles majeurs de la coagulation du sang et la présence d'une ascite abondante
EN PRATIQUE …
L’examen nécessite une courte hospitalisation de 12 à 24 heures
Un bilan sanguin est toujours fait avant la biopsie (quelques jours avant l’examen ou le matin même) afin de vérifier votre coagulation. On vous demandera d’arrêter l’aspirine, les antiagrégants plaquettaires ou les anticoagulants, si vous en prenez.
La biopsie hépatique est faite alors que vous êtes allongé dans un lit. Après un repérage échographique, le médecin effectue une anesthésie locale. Lorsque la zone de ponction est anesthésiée, le médecin réalise le prélèvement, entre les côtes, à l’aide d’une aiguille. Un petit fragment de foie est prélevé. Le geste dure à peine quelques secondes et est habituellement indolore.
Les 6 heures suivantes, vous devez rester allongé(e) sur le dos sur le lieu de l’examen.
Au bout de combien de temps a-t-on les résultats ?
Ils seront disponibles dans les 10 jours. Ils sont ensuite transmis à votre médecin traitant et au médecin qui a prescrit la biopsie.
Les complications possibles
Il est assez fréquent de ressentir une douleur modérée au niveau de la ponction ou de l’épaule droite dans les heures qui suivent. Ces douleurs passagères sont rapidement soulagées par la prise de paracétamol. Elles sont très rares. On peut observer exceptionnellement un hématome, une hémorragie (hémopéritoine), un épanchement de bile (cholé-péritoine), un pneumothorax (présence d'air dans la plèvre), une fistule artério-portale, une hémobilie (sang dans la bile). Ces accidents sont exceptionnels.
Important...
Une biopsie « négative » n’élimine pas totalement le diagnostic de cancer. En cas de biopsie négative d'un nodule suspect, une deuxième biopsie doit être envisagée. Après deux biopsies négatives les malades doivent être suivis par échographie et/ou scanner ou IRM tous les 3 à 6 mois jusqu'à ce que le nodule disparaisse, augmente de taille ou remplisse les critères en faveur d'un cancer.
Les recommandations du Thésaurus National de Cancérologie Digestive
| Nodule 1 à 2 cm | Nodule > 2 cm |
|---|---|
|
Scanner + IRM (ou échographie de contraste) |
Scanner ou IRM + alpha-foetoprotéine |
Que penser des marqueurs ?
LES BIOMARQUEURS SÉRIQUES
Trois biomarqueurs sériques pour préciser le risque de cancer du foie...
Ils ont été évalués pour déterminer le risque de cancer du foie dans les populations à haut risque : l’α-foetoprotéine (AFP), le rapport entre l’AFP lécithinique et l’AFP totale (AFP-L3) ainsi que la des-gamma-carboxy-prothrombine (DCP).
La réponse à cette question n'est pas claire car la plupart des études sur la performance des biomarqueurs dans la détection du CHC n’ont pas été effectuées dans un cadre de surveillance, mais ont comparé les concentrations de biomarqueurs chez les patients atteints de CHC avec un groupe témoin, le plus souvent représenté par des patients souffrant de maladies chroniques du foie.
L’α-foetoprotéine (AFP)
C'est le marqueur sérique le plus fréquemment utilisé pour la surveillance du cancer du foie, bien que tous les CHC ne libèrent pas de l’AFP dans la circulation sanguine.
Sa valeur diagnostique est plus sujette à controverse. De ce fait, le dosage de l’AFP n’est pas recommandée en combinaison avec l’échographie pour le diagnostic du CHC.
Le rapport de l’AFP glycosylée (fraction L3) sur l’AFP totale
Ce rapport est proposé pour la prédiction précoce du développement du CHC chez les patients souffrant d’une hépatite B ou C chronique. Une étude a montré que chez des sujets avec des concentrations faibles d’AFP et une échographie normale, une élévation de la’AFP-L3 permettait de prédire le développement du cancer un an avant le diagnostic chez un tiers des patients.
La des-gamma-carboxyprothrombine (DCP) ou prothrombine induite en l’absence de vitamine K II (PIVKA II)
C'est un autre marqueur sérique utilisé pour la surveillance des patients à risque et le diagnostic des cancers du foie, y compris dans les premiers stades.
Des concentrations sériques et tissulaires anormalement élevées de PIVKA-II ont été associées à la présence d’une invasion tumorale micro-vasculaire et à un facteur de risque de récidive tumorale et de mortalité.
LES BIOMARQUEURS GENETIQUES
Des biomarqueurs génétiques ont été décrits récemment et sont en cours d’évaluation. Une classification moléculaire des cancers du foie, basée sur les signatures génétiques ou des anomalies moléculaires, est en cours de validation pour une amélioration de la prise en charge des patients. Cependant, elle n’est pas suffisamment avancée pour être appliquée à la pratique clinique.
Mise à jour
1er août 2022

