Métastases cérébrales
Une métastase
Historiquement, le terme métastase, du grec metastasis « je change de place », est apparu au XVIème siècle pour désigner les tumeurs secondaires à une tumeur primitive. Ce phénomène est individualisé en tant qu’objet de recherche à partir de 1889, date de la publication dans The Lancet par J. Paget de l’hypothèse "seed and soil" [voir plus bas].
Actuellement, le processus métastatique est défini comme "une dissémination de cellules néoplasiques dans un site secondaire (ou de plus grand ordre) non contigu et distant, au sein duquel ces cellules prolifèrent pour former une masse extravasculaire de cellules incomplètement différenciées.
Les métastases cérébrales représentent la majorité des tumeurs intracrâniennes.
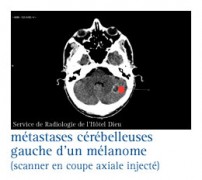
C'EST FRÉQUENT AU COURS DES CANCERS
GLOBALEMENT
Les métastases cérébrales représentent la troisième maladie neurologique en termes d’incidence avec plus de 30 000 nouveaux patients par an en France.
On estime que plus de 20 % des patients souffrant d'un cancer sont susceptibles d'en développer. Leur incidence à tendance à augmenter passant de 7 à 10 patients pour 100 000 entre 1987 et 2006, selon des statistiques suédoises.
L’âge au diagnostic des métastases cérébrales est d’environ 63 ans. Néanmoins, il est variable d’un cancer à l’autre : 40 à 49 ans pour le cancer du poumon, de 50 à 59 ans pour les cancers colorectaux et les cancers du rein et le mélanome
Le cancer du sein présente une incidence plus élevée dans la tranche d’âge la plus jeune, 20 à 39 ans.
Les métastases sont uniques dans seulement un tiers des cas. Les études scientifiques révèlent, aussi, que dans près de 80% des cas il existe moins de trois métastases.
LES DONNEES RECENTES
Dans le cas des cancers du sein, les tumeurs HER2 positives et triple-négatives sont les plus susceptibles de développer des métastases cérébrales.
Les métastases cérébrales du mélanome sont plus souvent associées à des mutations impliquant les gènes CDKN2A, BRAF, NRAS et.
Les métastases cérébrales des cancers du poumon sont souvent associées à des mutations des gènes EGFR et ALK. Les analyses moléculaires récentes ont également permis d'identifier des gènes non seulement associés à la formation et à la croissance du cancer du poumon, mais aussi spécifiques au risque de développer des métastases cérébrales, tels que le suppresseur de tumeur LKB1 et KRAS97.
Les métastases cérébrales des cancers du rein existe dans les trois principaux types histologiques de cancer du rein, les sous-types à cellules claires, papillaires et chromophobe.
Les facteurs mutationnels sont mieux caractérisés pour le sous-type à cellules claires, l'inactivation du gène suppresseur de tumeur VH. C’est la mutation la plus courante dans le cancer à cellules claires familial et sporadique. De plus, des sous-types moléculaires associés à différents pronostics cliniques ont été identifiés pour ce même type de cancer.
QUELS CANCERS PRIMITIFS ?
Bien que n'importe quel cancer puisse métastaser dans le cerveau, le risque de développement de lésions cérébrales est très important dans le cancer du poumon (incidence de 20 à 56 % selon les études) et significatif en cas de mélanome (7 à 16 %), de cancer du rein (6,5 %) ou de cancers colorectaux (2 %). Néanmoins, elles être diagnostiquées dans d'autres types de tumeurs, y compris les cancers du sang (hémopathies).
Pour le cancer du sein, l’incidence des métastases cérébrales varie de 5 à 20 % selon les études. Elle est également en relation avec le sous-type histologique. Certaines études rapportent une incidence de métastases cérébrales de 36 % dans les formes HER2 positives ainsi que dans le cas des cancers dits "triple négatifs"...
POURQUOI ?
À l’état physiologique, 15 % du flux sanguin irrigue le cerveau...
Les lieux privilégiés de dissémination métastatique sont les zones cérébrales très irriguées :
-
Les hémisphères cérébraux, en particulier au niveau de la jonction substance grise-substance blanche (80 %)
-
Le cervelet (15 %)
-
Le tronc cérébral (3 %).
Cependant, un tel phénomène, purement mécanique, n’explique cependant pas le tropisme cérébral variable des différents cancers.
Les cellules métastatiques d'une tumeur au cerveau ressemblent aux cellules de l'organe de la tumeur initiale et non aux cellules du cerveau. Par exemple, si une tumeur a commencé dans le sein et s'est étendue au cerveau, les cellules de la tumeur cérébrale ressembleront à des cellules anormales du sein et non à des cellules anormales du cerveau.
À QUEL ENDROIT DU SYSTEME NERVEUX ?
Dans plus des trois quart des cas, elles siègent dans les hémisphère cérébraux. Beaucoup plus rarement, elles affectent le cervelet (15 % des cas) ou le tronc cérébral (5 % des cas). Elles sont souvent multiples.
Elles se développent à la jonction de la matière grise et de la substance blanche.
Diagnostic
Les grandes lignes des traitements
LE CONTEXTE
Le traitement actuel des métastases cérébrales comprend généralement une combinaison de chirurgie (pour le diagnostic tissulaire, la décompression cérébrale et la survie prolongée lorsqu'elle est associée à une radiothérapie adjuvante dans certains cas) par rapport à la radiothérapie autonome et/ou aux thérapies médicales systémiques, dans le but global de sélectionner le ou les traitements optimaux pour un patient individuel afin de maximiser la qualité de vie et la survie globale.
Bien que les traitements curatifs restent aléatoires dans la plupart des cas après un diagnostic de métastases cérébrales, la décision thérapeutique tient de plus en plus compte de la survie anticipée, des risques des traitements et des toxicités à long terme lors du choix parmi les options de traitement disponibles. Ils peuvent être divisés en deux grandes catégories :
- la prise en charge symptomatique
- Les traitements ciblant les tumeurs.
LES TRAITEMENTS SYMPTOMATIQUES
Les corticostéroïdes, tels que la dexaméthasone
Ils représentent le principal traitement symptomatique en plus des analgésiques et sont souvent prescrits en réponse à des signes d'augmentation de la pression intracrânienne (HIC = Hypertension IntraCrânienne) ou d'œdème péri-tumoral symptomatique. En raison de l'importance de l'immunité dans la physiopathologie de la maladie métastatique, 'immunosuppression associée aux stéroïdes, la tendance actuelle est de minimiser l'exposition aux stéroïdes et à envisager des solutions de rechange à la corticothérapie.
Les antiépileptiques prophylactiques
Ils sont souvent prescrits comme agent symptomatique supplémentaire dans le but de réduire le risque de convulsions chez les patients atteints de métastases cérébrales. Cependant, les données récentes de méta-analyses ne soutiennent pas cette pratique en raison de l'efficacité préventive relative de ces médicaments.
LA CHIMIOTHERAPIE
Les agents systémiques traditionnels jouent un rôle limité dans la prise en charge des métastases cérébrales en raison de leur faible diffusion dans le cerveau et de l'imperméabilité de la barrière hémato-méningée. De plus, des pressions élevées de liquide interstitiel et une perfusion locale anormale affectent la diffusion dans la tumeur de la chimiothérapie.
Les approches expérimentales visant à résoudre ces problèmes comprennent l'administration assistée par convection qui utilise des cathéters placés stéréotaxiquement et une pression hydrostatique pour délivrer des agents antitumoraux directement dans le lit tumoral.
Plusieurs protocoles de chimiothérapie ont été évalués pour les cancers les plus courants avec métastases cérébrales.
Les agents cytotoxiques ont une efficacité modeste mais les associations cisplatine/pemetrexed, cisplatine/vinorelbine, paclitaxel/cisplatine semblent plus efficace. Le rôle du témozolomide est discuté. L’association chimiothérapie et radiothérapie semble plus performante.
LA NEUROCHIRURGIE
Une résection neurochirurgicale d'une métastase peut être utile chez certains patients présentant des métastases cérébrales pour plusieurs raisons :
- le diagnostic tissulaire,
- la décompression cérébrale pour diminuer l’hypertension intracrânienne
- la réduction de l'effet de masse symptomatique et l'œdème vasogénique
Elle offre une survie prolongée lorsqu'elle est suivie d'une radiothérapie adjuvante.
De plus, le profilage moléculaire de la tumeur pour aider à guider le choix d'un traitement
Les nouvelles approches thérapeutiques
LES THERAPIES CIBLEES
En cas de cancer du poumon
A partir de plusieurs études, il a été démontré que de nombreux anti-EGFR et anti-ALK ont une bonne pénétration dans le SNC, permettant des taux de réponse de plus de 40 % dans les cancers du poumon avec une mutation EGFR ou ALK.
L'osimertinib de troisième génération, qui cible également les cellules porteuses de la mutation T790M de l'EGFR (un mécanisme de résistance couramment acquis), a montré une meilleure pénétration de la BHE par rapport aux ITK de première génération
Chez les patients atteints de métastases cérébrales NSCLC ALK-positives, l'inhibiteur de première génération de l'ALK, le crizotinib, a montré des taux de réponse de 18 % malgré une pénétration limitée de la BHE.
Les nouveaux inhibiteurs d'ALK tels que l'alectinib, le céritinib, le brigatinib et le lorlatinib ont amélioré leur capacité à traverser la BHE, ce qui entraîne une augmentation de l'activité intracrânienne. Les inhibiteurs d'ALK semblent également être efficaces, quel que soit le moment de l'initiation.
Pour les patientes atteintes de métastases cérébrales dues au cancer du sein
En cas de cancer HER2+, le trastuzumab, un anticorps monoclonal anti-HER2 a une pénétration limitée de la BHE.
Le nératinib (un double inhibiteur de HER2 et de l'EGFR) est plus susceptible de traverser la BHE a donné des résultats en association avec la capecitabine. Le lapatinib a également une activité limitée en tant qu'agent unique et a donc été principalement utilisé en association avec capecitabine.
Chez les patientes atteintes de métastases cérébrales du cancer du sein ER-positives ou PR-positives, des études préliminaires ont fait état d'une pénétration adéquate du SNC et d'une efficacité potentielle des inhibiteurs sélectifs oraux des protéines du cycle cellulaire CDK4 et CDK6 (comme l'abémaciclib).
Les thérapies ciblées se sont également révélées prometteuses pour le traitement du mélanome.
Chez les patients atteints de métastases cérébrales dues à un mélanome avec mutation BRAF, l'utilisation des inhibiteurs de BRAF vemurafenib et dabrafenib en monothérapie a démontré des taux de réponse compris entre 20 % et 38 %
L'IMMUNOTHERAPIE CIBLEE
Des inhibiteurs des points de contrôle immunitaires ciblant les protéines de surface des lymphocytes impliqués dans l'immunité, CTLA4 (ipilimumab), PD-1 (pembrolizumab et nivolumab) ainsi que l'anti--L1 (atezolizumab) ont été surtout évalués chez des patients atteints de cancer du poumon et de métastases cérébrales de mélanome.
L'ipilimumab en monothérapie pour les métastases cérébrales du mélanome a entraîné des taux de contrôle de la maladie de 10 % chez les patients sous stéroïdes pour un œdème cérébral et de 25 % chez ceux qui n'étaient pas sous stéroïdes. En monothérapie le pembrolizumab est associé à un taux de réponse intracrânienne prolongé de 33 % dans le cancer du poumon et de 22 % dans le mélanome. Les schémas thérapeutiques combinés d'ipilimumab et de nivolumab chez des patients atteints de métastases cérébrales de mélanome ont montré des taux de réponse intracrânienne encore plus élevés, approchant les 60 %. La survie globale dans un essai était de 81,5 % à 1 an et de ~70 % à 2 ans. Ceci représente une amélioration drastique par rapport à la survie globale médiane de 4 à 5 mois chez les patients atteints de métastases cérébrales de mélanome de l'ère pré-immunothérapie.
Mise à jour
7 mai 2025

