Étude DUO-O
Fiche descriptive de l'étude
Étude ovaire
DUO-O
Titre de l'étude
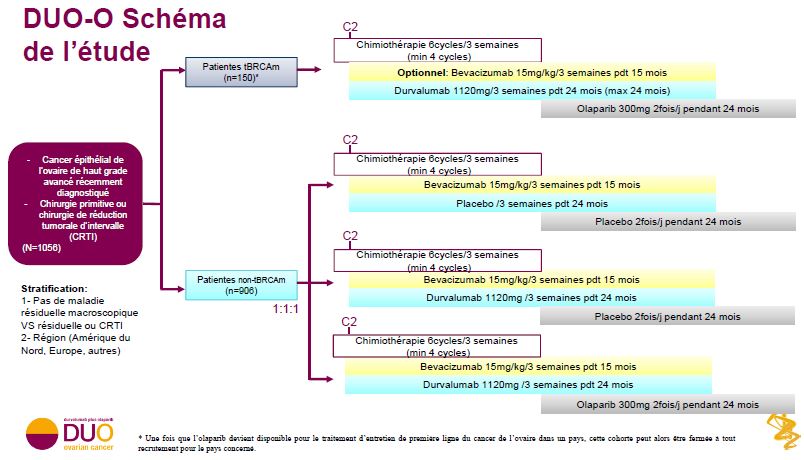
DUO-O : Étude multicentrique de phase III, en double-aveugle, contrôlée versus placebo, évaluant le durvalumab en association à une chimiothérapie et au bévacizumab, suivi d’un traitement d’entretien par durvalumab, bévacizumab et olaparib chez des patientes ayant un cancer de l’ovaire avancé récemment diagnostiqué.
Statut
Recrutement terminé / suivi en cours
Plan de traitement de l'étude
Promoteur
AstraZeneca
En collaboration avec le réseau ENGOT et ARCAGY-GINECO.
But
OBJECTIF PRINCIPAL
Evaluer l’efficacité et la tolérance de l’association du bévacizumab à un traitement de référence sous forme de chimiothérapie à base de platine, suivie d’un traitement de maintenance par bévacizumab soit en monothérapie soit en association au durvalumab, ou en association au durvalumab et à l’olaparib chez des patientes non-tBRCAm ayant un cancer de l’ovaire avancé récemment diagnostiqué. L’étude inclus également une cohorte en ouvert, pour déterminer le bénéfice potentiel de l’addition d’un traitement par durvalumab à la chimiothérapie de référence à base de platine et l’olaparib en traitement de maintenance.
PRINCIPAUX OBJECTIFS SECONDAIRES
- Survie globale,
- Tolérance,
- Taux de réponses objectives,
- PFS2,
- Temps entre la randomisation et l’initiation d’une 2nde et d’une 3ème ligne de traitement,
- Qualité de vie.
Phase
Phase III
Type de patiente
Patientes ayant un cancer épithélial de l’ovaire de haut grade (Stade FIGO III-IV) récemment diagnostiqué (y compris cancer péritonéal et/ou des trompes), ayant bénéficié au préalable d’une chirurgie ou prévoyant de commencer une chimiothérapie suivie d’une chirurgie de réduction tumorale d’intervalle.
Nombre de patientes recrutées
1056 dans environ 30 centres
72 patientes en France dans 11 centres
Critères d'évaluation
La durée entre la randomisation et la première progression (caractérisée par RECIST 1.1) ou le décès.